神経膠腫(グリオーマ)
1.神経膠腫(グリオーマ)とは?
- グリオーマとは、脳の中のグリアという細胞が腫瘍化したもので、10万人あたり3人程度に発生する脳腫瘍です。神経膠腫は最も多い脳腫瘍の一つであり、様々な性質をもった腫瘍が含まれます。
- 頭痛や吐き気、痙攣で初めて診断されることもありますが、手足の麻痺や言葉がでにくい失語症状、記憶力や計算力が落ちる高次脳機能障害がでることがあります。
- 脳腫瘍分類では、成人に発症する神経膠腫の多くは、低悪性度の星細胞腫(アストロサイトーマ)、乏突起膠細胞腫(オリゴデンドログリオーマ)、そして最も悪性度の高い膠芽腫(グリオブラストーマ)に分類されます。いずれも脳という重要な臓器に浸潤性に浸潤していき、脳機能障害をもたらすという点で悪性といえる性質を持っています。脳にしみこむように成長するため、全てを手術で摘出することは難しいことが多いです。
- 基本的には腫瘍組織の病理診断が悪性度分類に重要であり、悪性度分類はグレード2、3、4があり、4が最も悪性度が高いものになります。
- 膠芽腫グレード4の平均余命は2年くらいです。
- 毛様細胞性星細胞腫(グレード1)は全く違うものですから、この仲間に入りません。
- 従来グレードの脳腫瘍分類は、腫瘍の病理所見のみ決められてきましたが、近年は遺伝子異常の情報も重要であることがわかり、遺伝子異常も検討することが望ましいです。
- IDH遺伝子という遺伝子に異常がある場合には、比較的おとなしい性質を持つ星細胞腫(アストロサイトーマ)、乏突起膠細胞腫(オリゴデンドログリオーマ)であると考えられますが、これらの腫瘍の悪性度の幅は広く、悪性度が高い腫瘍もあるので注意が必要です。
- IDH遺伝子に異常がない場合は、多くの場合は悪性度が高いことが予測され、WHO2021脳腫瘍分類ではたとえ病理像が膠芽腫像でなかったとしても、実際には最終的には膠芽腫に含まれるという考え方もでてきています。
- 仮に低悪性度グリオーマであっても、いずれはゆっくりと進行していき、最終的には悪性化して致命的となることがあるため、グリオーマの適切な診断・治療が必要です。
2.グリオーマの診断
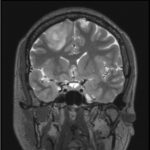
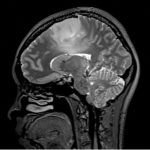
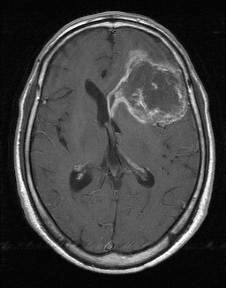
- 頭CT検査や頭MRI検査で見つかることが多く、画像検査のみでおおよそ診断できることが多いです。
- 腫瘍の代謝情報を得るためにメチオニンPET検査を行うことがあります。
- 当院では2024年12月より、アミノ酸代謝の多い領域の確認ができる、フルシクロビンPET検査を行えるようになりました。
- これらの画像検査でグリオーマが疑われた場合はまず腫瘍の診断と治療のために手術を行うことを検討します
3.手術
- 全てのグリオーマにおいて、最大限の外科的切除を行なうことが重要です。
- 膠芽腫の場合、腫瘍の約8割以上を摘出すると治療成績がよくなることが報告されています。
- 摘出が困難と考えられるようであれば、脳の安全な場所から少量の腫瘍を採取して診断をつける生検術を行うこともあります。
- 脳には機能(運動機能、言語機能、高次脳機能)がありますので、神経機能を温存した手術を行うことが重要です。
- そのためには、ニューロナビゲーションシステムを使用しながら、術中電気生理学的モニタリング、覚醒下手術、蛍光標識薬(5-ALA)などを駆使して、最大限の脳腫瘍摘出と、最小限の合併症を目指した手術を行っています。
- 手術中に全身麻酔を中断し、覚醒状態で言語機能等を確認しながら摘出を行う覚醒下手術は重要となってきています。
4.化学療法・放射線治療
星細胞腫(グレード3)
- 退形成性星細胞腫の標準治療を決めるための多くの試験が世界中で行われていますが、今のところ、グレードが3以上であれば膠芽腫に準じたテモゾロミド併用放射線治療が行われることが多いです
- IDH遺伝子に変異がなければ、全摘出できたとしてもグレード3であった場合は、膠芽腫に準じたテモゾロミド併用放射線治療を考慮します。
乏突起膠腫(グレード3)
- グレード3の場合は欧米では放射線治療を併用したPCV療法が有用であることが報告され、広く行われています
- 日本ではPCVのC(CCNU)の薬剤が使用できないため、似た薬剤であるACNU(A)もしくはMCNU(M)に変更したPAV, PMV療法が行われます
- グレード3であればテモゾロミド併用放射線治療も行うことができ、日本では多く行われています
*2023年に、IDH阻害薬:ボラシデニブ vorasidenib(飲み薬)の臨床第3相試験の結果が発表され,無増悪生存期間の延長が証明されました。米国で認可されましたので、もうすぐ日本でも使用できるようなります。
膠芽腫(グレード4)
- 標準治療はテモゾロミド内服治療を併用した放射線治療を行います。
- 放射線治療は平日毎日治療を行い、計30回、約1か月半の治療です。
- 高齢者の場合は15回もしくは5回に減量した放射線治療でも近い効果が得られることが明らかになり、広く行われつつあります。
- 放射線治療終了後は約1ヶ月(28日間)の内にテモゾロミドを5日間内服する維持療法を行います。
- アバスチン(ベバシズマブ)は膠芽腫に対しては再発時に使用すると生存期間が延長します。
- 初発時放射線治療時から併用しても生存期間は延長しません
- ただし、脳浮腫が強く症状が強い場合には、初発時でも症状が良くなる可能性があります。
- 手術で摘出を行った後に摘出腔の壁にギリアデル(カルムスチン脳内留置用剤)を直接置きます。
- オプチューン(電場腫瘍治療)は、電極パッド(アレイ)を頭皮に貼付け、電流を流し続ける治療です。
- テモゾロミド併用放射線治療が終了後、4-7週後より治療を開始します。
- 頭皮の皮膚炎には注意が必要ですが、その他には副作用の少ない新しい治療法です。
5.がんゲノムパネル検査を用いた新規阻害薬治療
- 遺伝子検査であるがんゲノムパネル検査が保険診療で行うことができるようになりました
- 脳腫瘍でも治療標的となる遺伝子異常が見つかった場合には治療薬を使える可能性があります
- 膠芽腫(グリオブラストーマ)で条件を満たせば保険診療で使用できる薬剤はキイトルーダ(ペンブロリズマブ)やロズリートレク(エヌトレクチニブ)等が挙げられます
- その他にも治験や患者申出治療として使用可能な薬剤もあります